La prématurité correspond à 11 % des naissances vivantes à l’échelle mondiale. Elle est spontanée dans 70 % des cas.
Une naissance prématurée a lieu avant le terme de la grossesse qui correspond à 41 semaines d’aménorrhée, soit 9 mois et demi à compter de la date des dernières règles. Un enfant est considéré comme prématuré s’il nait avant 37 semaines d’aménorrhée (SA), soit à 8 mois et demi de grossesse.
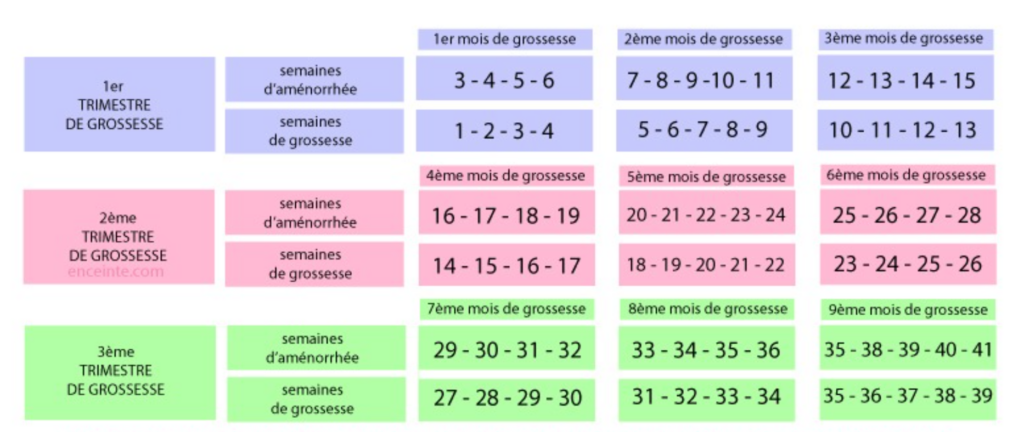
Deux techniques pour calculer l’âge gestationnel qui correspond toujours à 2 semaines de plus que la date de début de grossesse. Il est mondialement admis de parler d’âge gestationnel en SA, et non en semaines de grossesse.
- Compter les jours et les semaines à partir du 1er jour des dernières règles. En cas de cycle régulier, cela correspond à une grossesse qui débuterait à 2 SA, l’ovulation survenant en théorie 14 jours après le 1er jour des règles.
- Technique échographique: échographie T1 ( à 12 SA) : mesure de la longueur craniocaudale embryonnaire permet de dater précisément (à plus ou moins 3 j) le début de grossesse. On ajoute à cette date 2 semaines pour obtenir l’âge en SA.
Les niveaux de prématurité
On distingue trois niveaux de prématurité :
- la prématurité moyenne qui correspond à une naissance intervenant entre la 32e et la 36e semaine d’aménorrhée révolue (7 mois à 8 mois de grossesse),
- la grande prématurité correspondant à une naissance intervenant entre la 28e et la 32e SA (6 mois à 7 mois de grossesse),
- et la très grande prématurité pour les naissances intervenant avant 28 semaines, soit en deçà de 6 mois de grossesse.
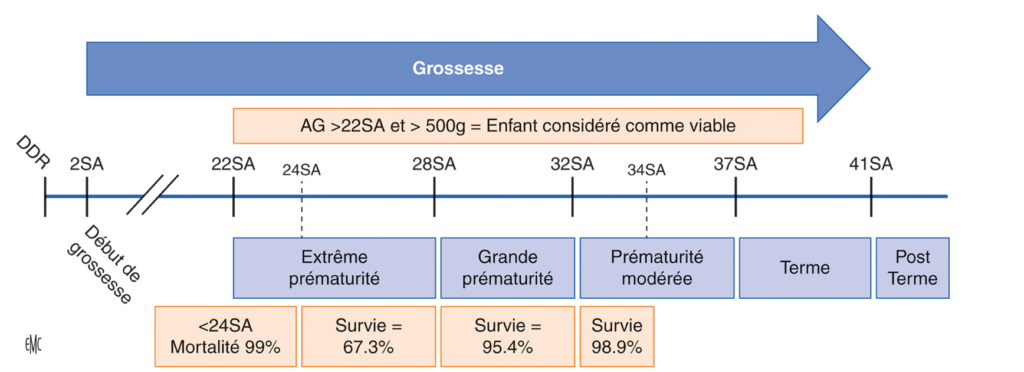
. DDR: dernier jour des règles; SA: semaines d’aménorrhée.
En France et dans de nombreux pays développés, le taux de naissances prématurées est en hausse ces dernières années. La prématurité est passée de 5,9% des naissances en 1995 à 7,4% en 2010. Entre 50 000 et 60 000 enfants naissent prématurément chaque année. Parmi eux, 85% sont des prématurés moyens (32-37 SA), 10% sont des grands prématurés (28-32 SA) et 5% sont des très grands prématurés, nés à moins de 28 SA.
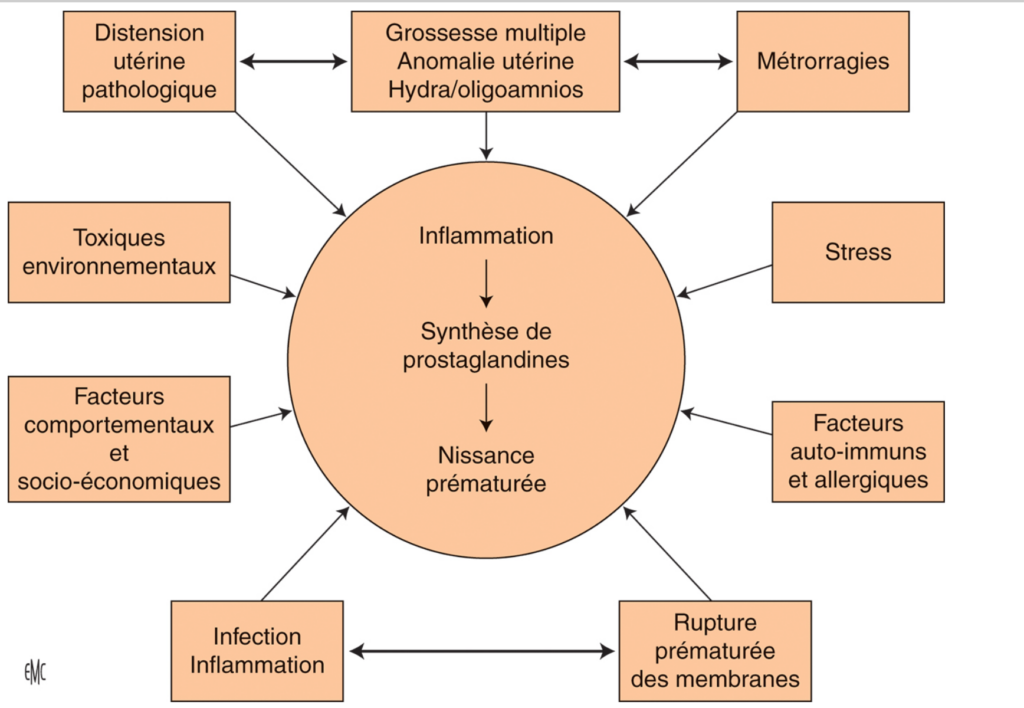
Des causes multiples
Environ 50% des naissances prématurées sont spontanées, dues à des contractions précoces dont la cause est rarement identifiée, ou à la rupture prématurée des membranes (ces ruptures étant parfois d’origine infectieuse).
L’autre moitié des naissances prématurées correspond à des naissances provoquées. Il s’agit alors d’une décision médicale et la naissance a le plus souvent lieu par césarienne. Une naissance prématurée peut être décidée en raison d’un risque de décès du fœtus ou de la mère en cours de la grossesse. Ce risque peut être lié à un retard de croissance grave du fœtus, une hypertension artérielle sévère chez la mère, ou une hémorragie maternelle dont l’origine n’est pas toujours expliquée.
L’hypertension maternelle sévère représente environ 20% des motifs d’accouchements avant 32 semaines de grossesse. Elle peut en effet entraîner des complications graves comme la pré-éclampsie, caractérisée par des anomalies rénales, ou l’éclampsie qui se manifeste par des convulsions chez la mère en raison d’une souffrance cérébrale. Elle peut aussi entraîner des troubles hépatiques, une destruction des globules rouges et des plaquettessanguines.
Parmi les autres causes possibles d’accouchement prématuré, citons : les infections génito-urinaires ou généralisées, des anomalies de l’utérus et du placenta (comme le placenta prævia qui peut se compliquer d’une hémorragie), le diabète maternel ou encore l’hématome rétro-placentaire (décollement prématuré du placenta accompagné d’un hématome).
Un tiers des enfants prématurés sont issus de grossesses multiples.
D’autres facteurs comme les conditions socio-économiques défavorables, l’âge plus avancé des mères, le stress ou encore la consommation de tabac sont aussi impliqués. Ainsi, le taux de prématurité est deux fois plus faible chez les femmes cadres que dans la catégorie ouvrières et employées.
Se préparer à l’accouchement prématuré
Le suivi médical au cours de la grossesse permet de repérer des situations à risques et de dépister des complications susceptibles de conduire à un accouchement prématuré (retard de croissance, hypertension maternelle…). En cas de menace d’accouchement prématuré, une administration de corticoïdes dans les 10 jours précédents la naissance permet d’accélérer la maturation pulmonaire du fœtus, d’éviter dans certains cas des difficultés respiratoires et cérébrales néonatales ainsi que des décès. Dans ces circonstances, la mère doit être orientée vers une maternité de type III disposant d’un service de réanimation néonatale.
L’immaturité du nouveau-né prématuré et les soins correspondants
La naissance prématurée d’un enfant interrompt son développement in utero : ses organes sont présents mais ils sont immatures. Ceci concerne principalement quatre organes : le cerveau, les poumons, le tube digestif et le canal artériel.
Immaturité du système nerveux central
Bien que les structures cérébrales soient en place, le cerveau des grands prématurés est immature. Des étapes essentielles à son développement se produisent en effet entre la 24e et la 32e semaine de gestation. La naissance prématurée vient donc interrompre le processus normal de maturation et le développement cérébral optimal.
Une surveillance régulière par électroencéphalogramme et par l’imagerie est nécessaire au cours des premières semaines pour dépister d’éventuelles anomalies, en particulier en cas de grande prématurité.
En cas de menace d’accouchement prématuré, l’administration de corticoïdes à la mère réduit le risque d’hémorragie cérébrale chez l’enfant. Parfois associé, le sulfate de magnésium semble également réduire le risque de paralysie cérébrale.
Complications possibles sur le plan neurosensoriel:
- la rétinopathie du prématuré, caractérisée par une néovascularisation de la rétine, pouvant être à l’origine de troubles visuels à long terme,
- les hémorragies intraventriculaires, considérées comme sévère si elles sont de grade 3 (à l’origine de dilatation ventriculaire) ou de grade 4 (avec atteinte du parenchyme cérébral),
- les leucomalacies périventriculaires, pouvant évoluer vers des kystes de la substance blanche, et à risque de paralysie cérébrale.
Immaturité pulmonaire
Des poumons matures produisent une substance qui tapisse la surface des alvéoles pulmonaires et permet leur bon fonctionnement : le surfactant. Chez les prématurés, les poumons ne produisent pas encore cette substance, ce qui entraine des difficultés respiratoires. La possibilité de synthétiser le surfactant apparaît en moyenne après la 32e semaine, mais il existe une grande variabilité d’un enfant à l’autre.
Il est donc nécessaire d’administrer aux enfants prématurés un surfactant exogène, à l’aide d’une sonde d’intubation. Une assistance respiratoire sous forme de ventilation mécanique nasale ou par l’intermédiaire d’une sonde d’intubation est également utilisée pour pallier l’immaturité pulmonaire.
Malheureusement, chez certains enfants, la ventilation mécanique associée à l’immaturité pulmonaire se complique d’une inflammation et d’une hyperréactivité bronchique qui entraine une pathologie pulmonaire : la dysplasie broncho-pulmonaire. Cette complication constitue l’une des principales causes de morbidité chez les enfants prématurés.
Les prématurés nés à moins de 34 à 36 semaines de grossesse font par ailleurs fréquemment des pauses respiratoires (apnées) dues à l’immaturité de la commande neuro-respiratoire. Ces pauses peuvent entraîner une diminution de la quantité d’oxygène dans le sang nécessitant la mise en place d’une assistance respiratoire. Un traitement par un dérivé de caféine stimule les centres neuro-respiratoires. Il est systématiquement délivré aux grands prématurés.
Immaturité digestive
Le prématuré n’a pas encore le réflexe de succion et ses mécanismes de déglutition et de respiration ne sont pas coordonnés. Dès lors, avant un âge gestationnel de 34 semaines l’alimentation des enfants se fait par voie entérale, à l’aide d’une sonde introduite dans le tube digestif via la bouche. Le choix du lait dépend de l’âge gestationnel. Le lait maternel est recommandé, qu’il provienne de la mère ou de lactarium (banque de lait de femme). Il peut être enrichi. Il existe également du lait spécifique pour prématurés.
L’immaturité digestive peut se compliquer d’une maladie rare, mais mortelle et mal connue : l’entérocolite ulcéro-nécrosante. Elle correspond à une destruction du tube digestif. Si cette maladie ne concerne que 2% des grands prématurés, elle ne survient parfois que trois à quatre semaines après la naissance, alors que les soignants pensent que le plus difficile est derrière eux.
Autres immaturités
En raison d’une immaturité hépatique, les prématurés ont le plus souvent un ictère (jaunisse) qui débute vers le 2 ou 3e jour de vie et dure quelques jours. Il résulte de la dégradation naturelle des globules rouges. L’ictère est traité par photothérapie.
Les reins sont également immatures,ce qui nécessite de contrôler régulièrement le volume et le contenu des urines, pour adapter les besoins du nouveau-né en nutriments ou encore en érythropoïétine produite par les reins.
Il existe enfin une immaturité du système immunitaire qui peut entrainer des infections graves.
Parcours de soin du prématuré
La prise en charge de l’enfant dépend de son stade de prématurité. Les prématurés extrêmes et grands prématurés sont accueillis en service de réanimation néonatale où ils reçoivent les soins nécessaires et adaptés à leurs risques et bénéficient d’une surveillance renforcée. Ils sont ensuite orientés vers les soins intensifs, puis en service de néonatalogie quand leur état de santé est stable.
Les prématurés sont placés en couveuse pour les maintenir à 34°/35° C, température équivalente à celle du ventre de la mère. L’atmosphère de la couveuse doit par ailleurs présenter un taux d’humidité de 80 %. Les enfants peuvent sortir de couveuse à partir de 2 kg.
En outre, leur prise en charge doit s’intégrer dans le plus grand respect possible de leur rythme veille/sommeil, pour réduire le stress généré par les stimulations extérieures. Les soins de développement (dont la forme la plus aboutie est le NIDCAP) permettent d’individualiser au mieux cette prise en charge après une observation attentive du prématuré par les soignants. L’objectif de ces soins est de coller au plus près avec l’environnement intra-utérin : niveau bas de lumière, pas d’alternance jour/nuit, faible niveau sonore, postures respectant la position physiologique en flexion… Dans ce cadre, le contact avec les parents est très fortement encouragé sous forme de « peau à peau« . Ce contact rapproché rassure l’enfant, réduit son stress et favorise les montées de lait chez la mère. Les enfants ayant de nombreux contacts en « peau à peau » avec leurs parents ont une évolution plus favorable, avec une amélioration du rythme cardiaque, de la fréquence respiratoire ou encore du sommeil.
Généralement, un enfant peut sortir de l’hôpital lorsqu’il est devenu autonome du point de vue respiratoire et digestif. L’hospitalisation à domicile permet de raccourcir la durée d’hospitalisation.
L’évolution de l’état de santé dépend de chaque enfant et aucun marqueur ne permet de savoir avec précision si l’enfant va développer des complications et des séquelles à long terme. Certains facteurs sont néanmoins plus favorables : un âge gestationnel plus avancé, un poids supérieur à la normale pour l’âge gestationnel ou encore le fait d’être une fille. Il existe une relation continue entre l’augmentation de l’âge gestationnel et la baisse de la morbi-mortalité néonatale. Les risques de détresse respiratoire sévère ou d’atteinte neurologique, ainsi que les durées moyennes de séjour dans les unités d’hospitalisation néonatale diminuent avec l’âge gestationnel.
En France, aucune intervention n’est tentée sur les prématurés nés à 23 semaines de grossesse. La prise en charge d’un prématuré extrême résulte d’une décision collégiale, si les soignants la jugent pertinente et si les parents le souhaitent.
Les séquelles neurologiques sont fréquentes, en particulier chez les grands prématurés. Elles peuvent se manifester par des troubles moteurs avec un retard à la marche ou des difficultés à marcher, des troubles cognitifs avec des difficultés de langage oral ou écrit, ou encore des troubles de l’attention et des troubles sensoriels, visuels ou auditifs.
L’étude Epipage 1 menée en 1997 auprès de grands prématurés avait montré que près de 40% d’entre eux présentaient une déficience motrice, sensorielle ou cognitive à l’âge de cinq ans, contre 11% des enfants du même âge nés à terme. Au total, le risque de déficience était environ quatre fois plus élevé chez les grands prématurés, toujours par rapport aux enfants nés à terme. Toutefois, les formes sévères de déficiences ne concernaient que 5% des enfants. Après 32 semaines de grossesse, le risque de complications immédiates et à long terme est nettement réduit mais n’est pas nul : 4% des enfants nés à 32 SA présentent une paralysie cérébrale à 5 ans. Et les taux d’hospitalisations des enfants nés à 38 SA sont encore supérieurs à celui observé chez les enfants nés à terme (8,8% contre 6,4%). La prématurité modérée ne doit donc pas être banalisée.
Une amélioration significative entre 1997 et 2011
Le « paysage » de la prématurité ayant changé depuis 1997, avec une augmentation des cas et des évolutions dans les pratiques médicales en obstétrique et en néonatologie, une nouvelle étude a été mise en place depuis 2011 pour mettre à jour les données : Epipage 2. Les premiers résultats de cette étude montrent que le pourcentage de survie est de 59% à 25 SA, 75% à 26 SA, 94% entre 27-31 SA et 99% entre 32 et 34 SA. Quant aux taux de sortie de néonatalogie sans pathologie néonatale grave, il est de 30% à 25 SA, 48% à 26 SA, 81% entre 27-31 SA et 97% entre 32-34 SA. Avant 25 semaines de gestation le pronostic des enfants demeure très incertain. A ce jour, les premières données d’Epipage 2 montrent une amélioration significative de la survie et de la survie sans morbidité néonatale sévère chez les enfants nés entre 25 et 31 semaines depuis 1997.
Après la sortie de l’hôpital, la croissance staturo-pondérale du prématuré est plus rapide que celle de l’enfant né à terme. Par ailleurs, lorsque le pédiatre compare les acquisitions psychomotrices du prématuré à celles d’un nourrisson né à terme, il tient compte de « l’âge corrigé » et non de l’âge réel. Lorsqu’un prématuré est né après 7 mois de grossesse, on peut dire qu’il a 2 mois d’avance. Lorsqu’il aura civilement 10 mois, il aura 8 mois d’âge corrigé.
Sites à consulter:
https://www.sosprema.com/page/173829-la-prematurite
https://www.rp2s.fr/axes-thematiques/suivi-prematures-devenirp2s/
Particularités dans la prise en charge
1.Suivi réseau prématuré
Près de 40 Réseaux de Périnatalité couvrent le territoire français et sont représentés par la Fédération Française des Réseaux de Santé en Périnatalité (FFRSP). Toutes les maternités françaises sont rattachées à un Réseau de Périnatalité.
Le champ d’intervention de ces réseaux comprend le suivi de toutes les grossesses (normales ou pathologiques) en amont et en aval de la naissance, le suivi des nouveau-nés durant le 1er mois de vie, et jusqu’à 7 ans pour les nouveau-nés vulnérables.
Ils répondent à un cahier des charges national et leurs missions visent à améliorer la qualité des prises en charge et la sécurité en proposant au patient un réseau gradué de compétences de proximité.
Les réseaux interviennent essentiellement en appui aux professionnels de la périnatalité, par des actions d’information, de formation, d’évaluation et suivi des indicateurs. Ils sont également un interlocuteur des Agences Régionales de Santé (ARS) et participent à la politique de santé publique en périnatalité.
Les professionnels du réseau sont :
- médecins (gynéco-obstétriciens, pédiatres, généralistes, anesthésistes, pédopsychiatres…)
- sages-femmes
- puéricultrices
- auxiliaires de puériculture
- psychologues
2.Vaccinations:
Vaccins hexavalents
Chez le prématuré <33 SA: choix du protocole à 4 injections : 2, 3, 4 et 11 mois. (Recommandation du calendrier vaccinal : 2, 4, 11 mois ; conseil Infovac-GPIP : 2, 3, 4, 11 mois)
Enfant ≥ 33 SA : 3 injections 2, 4, 11 mois suffisent pour vaccins hexavalent.
Pour tous les enfants nés < 37 SA.
Pneumocoque 13 valences : recommandation 4 injections 2-3-4 et 11 mois
2. Dépistage ophtalmologique
3. Dépistage auditif